强酸和弱酸
酸是在溶液中混合时提供氢离子或质子的化学物质。由特定酸释放的质子数实际上决定了酸的强度 - 无论是强酸还是弱酸。为了理解酸的强度,需要比较它们向类似碱(主要是水)提供质子的倾向。强度由称为pKA的数字表示。

什么是强酸?
如果酸在溶液中完全解离或离子化,则称其为强酸。这意味着,当在溶液中混合时,它能够提供最大数量的H +离子或质子。这些离子是带电粒子。由于强酸在分解或离子化时会产生更多的离子,这意味着强酸是电的导体。
当酸混入H时2O,质子(H+ 离子)被带到H2O分子产生H3O+ (羟鎓离子)和a - 离子,以此为基础开始使用酸。
在一般情况下,

可以尊重这种化学反应,但在少数情况下,酸会释放出H+ 离子非常容易,反应看起来像是单向的。并且酸完全解离。
例如,当氯化氢溶解在H中时2为了制造HCl,我们可以写出很少的逆反应:

同时,将发生百分之百的虚拟反应,其中氯化氢将显示与H3O的反应+ (Hydroxonium ion)和Cl– 离子。这里,强酸是氯化氢。
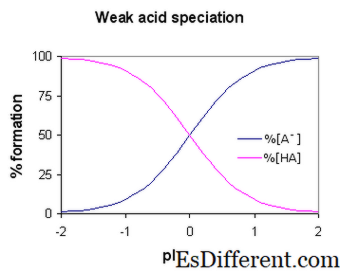
什么是弱酸?
如果酸部分或不完全电离,仅将一些氢原子释放到溶液中,则称其为弱酸。因此,与释放质子中的强酸相比,它的能力较差。弱酸具有比强酸更高的pKa。
乙酸是弱酸的一个很好的例子。它显示了与H的反应2O用于生产H3O+ (Hydroxonium离子)和CH3COOH(乙酸根离子),但反向反应比前进反应更成功。分子很容易反应以改善酸和H.2O.

在任何时候,只有约1%的CH3COOH酸分子显示转化为离子。剩下的是简单的乙酸(系统地称为乙酸)分子。
强酸和弱酸的区别
强酸
强酸是在水溶液中完全电离的酸。当溶解在H中时,强酸总是会使质子(A H +)松散2O.换句话说,强酸总是在它的脚趾上,并且非常有效地释放质子。
弱酸
弱酸是在溶液中部分电离的酸。它只能将少量氢原子释放到溶液中。因此它比强酸的能力低。
强酸
强酸总是表现出强导电性。与相同电压和浓度的弱酸相比,强酸通常会传递更多电流。
弱酸
弱酸具有低导电性。它们是导体不良并且电流通过的值很低
强酸
强酸中的反应速度更快
弱酸
弱酸中的反应速度较慢
强酸
盐酸(HCl),硝酸(HNO3),高氯酸(HClO4),硫酸(H2所以4),氢碘酸(HI),氢溴酸(HBr),氯酸(HClO3).
弱酸
亚硫酸(H2所以3),乙酸(CH3COOH),磷酸(H3PO4),苯甲酸(C6H5COOH),氢氟酸(HF),甲酸(HCOOH),亚硝酸(HNO2).
强酸
在强酸中,pH通常低于3.强酸具有非常高浓度的H +离子(pH为3的酸具有0.001摩尔/升氢离子)。
弱酸
弱酸的pH范围为3-7。
强酸
在强酸中,pKa的值非常低。
弱酸
在弱酸中,pKa的值非常高。
强酸
HCl(g)+ H2O(1)≈H3Ø+(aq)+ Cl−(水溶液)
弱酸
CH3COOH(1)+ H2O(1)≈H3Ø+(aq)+ CH3COO−(水溶液)
强酸的概述弱酸
强酸和弱酸的差异点总结如下:对比图